Un equipo del Hospital Johns Hopkins All Children’s encontró que “activar de manera directa” el microambiente inmunológico en tumores de ratón, mediante la coactivación de STING y LTβR, recluta rápidamente células T y B, forma centros inmunitarios dentro del tumor (TLS) y remodela los vasos sanguíneos tumorales en puertas de entrada para linfocitos. Crédito: Stock
Los científicos de Johns Hopkins descubrieron una forma de convertir tumores ‘inmunológicamente fríos’ en ‘inmunológicamente calientes’ al activar vías inmunitarias clave.
En estudios realizados con modelos de ratón de cáncer de mama, páncreas y músculo, los científicos del Hospital Johns Hopkins All Children’s han descubierto nuevas evidencias de que un enfoque único para estimular las defensas inmunitarias naturales del cuerpo puede ayudar a prevenir la recurrencia del cáncer y mejorar las tasas de supervivencia.
La investigación, publicada en Nature Immunology, recibió apoyo federal del Instituto Nacional del Cáncer/NIH. Los tumores cancerosos a menudo se etiquetan como “inmunológicamente fríos” o inmunosupresores porque el sistema inmunitario no los reconoce como amenazas. Como resultado, estos tumores resisten el ataque de las células inmunitarias y responden pobremente a los tratamientos estándar, lo que conduce a resultados menos favorables para los pacientes.
El equipo de Johns Hopkins se propuso encontrar una manera de transformar estos tumores inmunológicamente fríos en tumores “inmunológicamente calientes”, es decir, tumores que el sistema inmunológico pueda detectar y atacar. Su objetivo era hacer que las células inmunitarias, como las células B y las células T, fueran más efectivas para destruir las células cancerosas y mejorar la respuesta de los pacientes tanto a la quimioterapia como a la inmunoterapia.
Mejorando la inmunidad tumoral a través de la formación de TLS
Basándose en su investigación previa sobre el cáncer de mama, el equipo de investigación planteó la hipótesis de que “animar” el ambiente tumoral con agentes que activan el sistema inmunológico mejora la “aptitud” de las estructuras linfoides terciarias (TLS) y aumenta drásticamente las respuestas inmunitarias para atacar los tumores.Las TLS son grupos de linfocitos que se forman en áreas de inflamación crónica, incluidos los tumores inmune-calientes.
Estas estructuras son fundamentales para ayudar al sistema inmunológico a combatir el cáncer, y su presencia se correlaciona fuertemente con una mejor respuesta al tratamiento y la supervivencia del paciente.
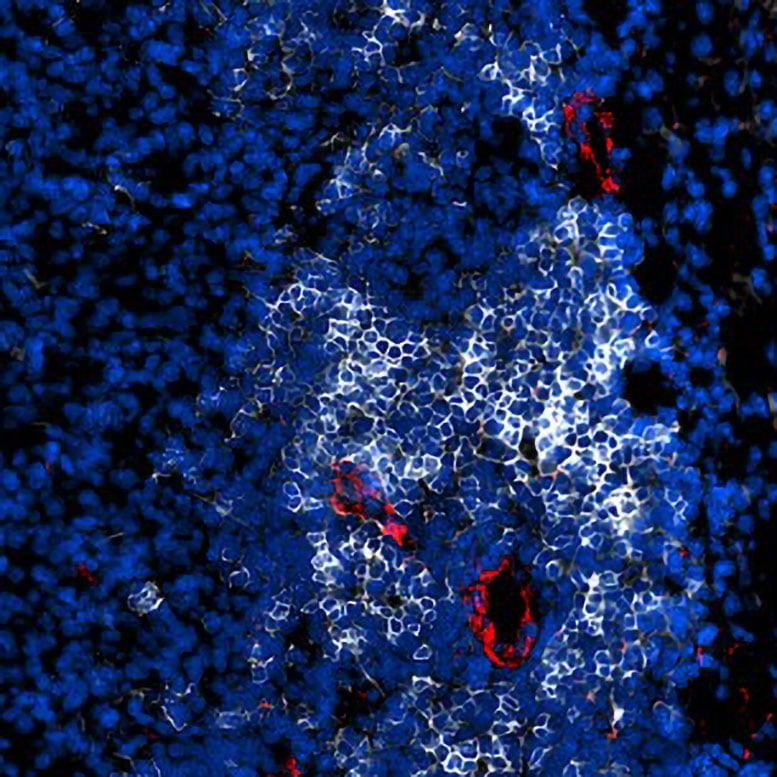
Una imagen de fluorescencia de una estructura linfoide terciaria (TLS), la estructura inmune similar a un ganglio linfático que se desarrolla en tumores. Las células B (blancas) están formando un agregado denso de TLS. Los vasos venosos endoteliales altos (rojos) que se desarrollan alrededor de los TLS son vasos sanguíneos especializados que funcionan como puertas de entrada de las células inmunitarias a los tumores, a través de los cuales las células B y T son reclutadas desde la circulación sanguínea hacia el tumor para combatir las células cancerosas. Crédito: Nature Immunology1
Para probar su enfoque, los investigadores “ingeniaron a la inversa” un entorno tumoral rico en TLS para identificar los estímulos necesarios para la formación de TLS. Luego aplicaron estos estímulos a tumores libres de TLS que crecían en ratones, administrando dos sustancias que activan el sistema inmunológico (agonistas) que estimulan la proteína STING y el receptor de linfotoxina-β (LTβR).
La activación dual de STING y LTβR provocó una respuesta rápida de las células T asesinas (células T CD8⁺), lo que llevó a una fuerte inhibición del crecimiento tumoral.
El tratamiento también indujo la formación de vénulas endoteliales altas, los vasos sanguíneos especializados que permiten la entrada de linfocitos en los tejidos. Estos vasos sanguíneos funcionaron como puertas dedicadas, permitiendo que grandes cantidades de células T y B ingresaran a los tumores y se ensamblaran en TLS.
Estableciendo una protección inmune a largo plazo
Dentro de estos TLS, las células B iniciaron reacciones en los centros germinales, maduraron hasta convertirse en células plasmáticas secretoras de anticuerpos y generaron células de memoria de larga duración. Se detectaron anticuerpos IgG específicos del tumor, y las células plasmáticas persistieron en la médula ósea, lo que constituye evidencia de una inmunidad sistémica y duradera que puede ayudar a proteger contra la recaída.
El tratamiento también aumentó las células T helper (CD4⁺) y las células T de memoria CD8⁺, y equilibró la señalización inmune, fortaleciendo tanto la inmunidad mediada por anticuerpos (humoral) como la inmunidad mediada por células.
En conjunto, dicen los investigadores, los hallazgos sugieren que los esfuerzos tempranos y combinados para aumentar la actividad de las células T no solo matan directamente las células tumorales, sino que también inducen la maduración de TLS que mantiene y amplifica las respuestas antitumorales.“
Nuestros hallazgos muestran que podemos inducir terapéuticamente TLS funcionales en tumores que de otro modo serían inmunológicamente fríos”, dice Masanobu Komatsu, Ph.D., investigador principal del estudio y científico senior en el Instituto Johns Hopkins All Children’s Cancer & Blood Disorders.
“Al construir la infraestructura inmune adecuada dentro de los tumores, podemos potenciar las propias defensas del paciente, tanto las células T como las células B, contra el crecimiento del cáncer, la recaída y la metástasis.”
Dado que la abundancia de TLS se correlaciona con mejores resultados en muchos tipos de tumores, el uso conjunto de los dos estimuladores de proteínas podría ofrecer una forma ampliamente aplicable de mejorar la eficacia de las terapias existentes, incluidos los inhibidores de puntos de control que son la base de las inmunoterapias, y la quimioterapia tradicional.
El equipo de Komatsu está investigando además el mecanismo de acción de la terapia TLS y se está preparando para su aplicación clínica en pacientes adultos y pediátricos con cáncer.
Fuente: Esta investigación fue apoyada por las subvenciones R01 del Instituto Nacional del Cáncer/NIH, el Programa de Investigación del Cáncer Dirigido por el Congreso del Departamento de Defensa, y el Programa de Investigación del Cáncer Bankhead Coley del Departamento de Salud de Florida.
Este articulo llega a ustedes gracias al patrocinio de Productos Caribena.

